
英国警示贝利木单抗严重精神不良事件发生增加的风险
2019年4月,英国药品和健康产品管理局(MHRA)发布信息称,包括一项随机临床试验在内的临床试验初步结果显示,接受贝利木单抗的系统性红斑狼疮患者与那些除标准治疗外接受安慰剂治疗的患者相比,有增加抑郁、自杀意念/行为、或自我伤害的风险。
贝利木单抗是人源 IgG1λ单克隆抗体,特异性地针对可溶性人B淋巴细胞激活蛋白。贝利木单抗已批准用于已进行了标准治疗的、成人型活跃的自身抗体阳性的且伴随高疾病活动度的系统性红斑狼疮的辅助治疗(例如,阳性的抗dsDNA抗体和低补体情况下)。2018年,在英国贝利木单抗估算暴露量是102个患者年。
在利木单抗获批的临床研究中,与对照组相比,观察到精神不良事件发生率的失衡。评估发现贝利木单抗的获益大于风险。然而,作为附条件的上市许可,贝利木单抗的上市许可持有人被监管机构要求开展一项随机、安慰剂对照的临床试验(BEL115467),以评估本品的全因死亡率和预先指定的特别关注的不良事件,包括选定的严重精神不良事件。目前,该研究正在全球范围内开展。
该项研究的1年期数据初步显示,与标准治疗加安慰剂治疗的患者相比,标准治疗加贝利木单抗治疗患者报告更多的严重抑郁、自杀意念或行为及自我伤害(见表格)的不良事件(见下表)。
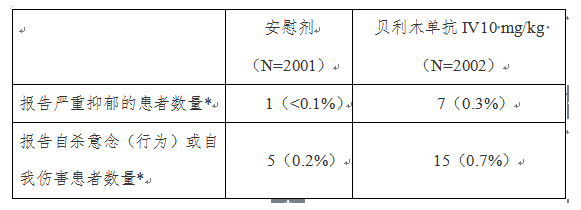
基于以上研究结果,在贝利木单抗治疗之前,建议考虑患者病史和目前精神状态,处方医生应仔细评估患者抑郁和自杀风险;如果患者出现新的或精神症状加重,建议患者尽快就医。
给医务人员建议:
包括一项随机临床试验在内的临床试验初步结果显示,接受贝利木单抗治疗的患者有增加严重精神不良事件(抑郁、自杀意念/行为[包括由自杀导致的死亡]、或自我伤害)风险。
在贝利木单抗治疗之前,考虑患者病史和目前精神状态,应仔细评估抑郁和自杀风险。
在治疗过程中,监测所有患者上述风险相关的新的或加重的症状。
如果患者出现了新的精神症状或精神症状加重,应评估继续治疗的获益和风险。
给患者(和看护者,如适用)建议:
正在使用贝利木单抗的患者,可能经历情绪或行为变化,如果出现了新的或加重的抑郁、自杀意念、或关于伤害自己的想法时应尽快就医。
患者可让家庭成员或朋友知悉他们正在使用贝利木单抗,这样家庭成员或朋友可以注意患者情绪上的任何变化。
-
安徽省药品质量公告 (2021年第3期,总第61期)
为加强药品质量监管,保障公众用药安全,根据安徽省药品抽检计划,全省各级药品监督管理部门和药品检验机构对本行政区域药品生产、经营企业和使用单位的药品质量进行了抽查检验。本期抽验信息共涉及392个抽样单位,430个药品生产企业的1322批次产品,检验结果1317批次产品符合规定,5批次产品不符合规定(相关检验结果仅对样品负责)。现予以公告。药品安全消费提示:居民用药请遵从医嘱,凭执业医师或助理医师开具的处方购买处方药;居民购药,请到持有《药品经营许可证》的药店购买;购药时,请索取并保存有效票据,要认真查看药品外包装盒上标注的药品通用名、标签、生产日期、批号和有效期等内容,仔细阅读药品使用说明书;购买药品后要按说明书标明的贮藏条件保存药品;如购买到假冒伪劣或质量不合格药品,请及时拨打当地市场监管部门举报投诉电话12315。不符合规定药品名单:
-
国家药监局关于15批次药品不符合规定的通告(2021年第49号)
经甘肃省药品检验研究院等7家药品检验机构检验,标示为安徽济善堂中药科技有限公司等14家企业生产的柴胡(北柴胡)等15批次药品不符合规定。现将相关情况通告如下: 一、经黑龙江省药品检验研究中心检验,标示为湖北科益药业股份有限公司生产的1批次喷昔洛韦乳膏不符合规定,不符合规定项目为性状。 经福建省食品药品质量检验研究院检验,标示为广东宏盈科技有限公司生产的1批次氯霉素滴眼液不符合规定,不符合规定项目为有关物质。 经山东省食品药品检验研究院检验,标示为江西药都樟树制药有限公司生产的1批次脑灵素胶囊不符合规定,不符合规定项目为水分。 经北京市药品检验所检验,标示为湖北济安堂药业股份有限公司生产的1批次心脑欣片不符合规定,不符合规定项目为重量差异。 经重庆市食品药品检验检测研究院检验,标示为九寨沟天然药业集团有限责任公司生产的1批次壮骨麝香止痛膏不符合规定,不符合规定项目为含膏量。 经湖北省药品监督检验研究院检验,标示为北京博爱堂安国中药科技有限公司生产的1批次苍术不符合规定,不符合规定项目为含量测定。 经甘肃省药品检验研究院检验,标示为广西蓝正药业有限责任公司、岷县归芪堂药业有限公司生产的2批次柴胡不符合规定,不符合规定项目为杂质;标示为河北悦康志德药业有限公司、安徽济善堂中药科技有限公司、亳州市张仲景中药饮片有限责任公司、广东天诚中药饮片有限公司生产的5批次柴胡(北柴胡)不符合规定,不符合规定项目为杂质;标示为湖南馨恒堂中药科技有限公司生产的1批次柴胡(醋柴胡)不符合规定,不符合规定项目为性状;标示为苏州市天灵中药饮片有限公司生产的1批次柴胡(根)不符合规定,不符合规定项目为杂质。 二、对上述不符合规定药品,药品监督管理部门已要求相关企业和单位采取暂停销售使用、召回等风险控制措施,对不符合规定原因开展调查并切实进行整改。 三、国家药品监督管理局要求相关省级药品监督管理部门依据《中华人民共和国药品管理法》,组织对上述企业和单位生产销售假劣药品的违法行为立案调查,并按规定公开查处结果。 特此通告。不符合标准规定药品名单:
-
甘肃省药品监督管理局药品质量公告
经兰州市食品药品检验检测研究院(原兰州市食品药品检验所)检验,标示为北京仟草中药饮片有限公司等3家企业生产的3批次药品不符合标准规定。现将相关情况公告如下:一、标示为北京仟草中药饮片有限公司等3家企业生产的3批次药品,经抽检质量不符合标准规定。二、对检验不符合标准规定的药品,相关市场监督管理部门已采取查封扣押等必要的控制措施,并依据相关法律法规对产品涉及单位已经或正在进行立案查处,将于三个月内公开处理结果。三、对不合格产品及涉及的相关单位,各市州市场监督管理部门要加强监管,督促其查明问题原因,制定落实整改措施,切实消除风险隐患。特此公告。不符合标准规定药品名单:
-
云南省药品监督管理局发布2021年第2期药品质量公告
为加强药品质量监管,保障公众用药安全,按照2021年云南省药品监督抽检计划,我省各级药品监督管理部门对全省药品生产、经营企业和使用单位的药品质量进行了监督抽检,现将药品抽检情况予以公告。不合格药品质量公告:










